Inhoud
- Dosering
- Aanbevelingen voorschrijven
- Vaak voorkomende bijwerkingen
- Geneesmiddelinteracties
- Contra-indicaties en overwegingen
Harvoni werd op 10 oktober 2014 goedgekeurd door de Amerikaanse Food and Drug Administration (FDA) voor gebruik bij volwassenen van 18 jaar en ouder met HCV genotypen 1-infectie, inclusief diegenen met cirrose.
Harvoni is goedgekeurd voor gebruik bij niet eerder behandelde ("behandelingsnaïeve") patiënten, evenals patiënten met een gedeeltelijke of geen respons op eerdere HCV-therapie ("eerder behandeld").
Harvoni is het eerste door de FDA goedgekeurde HCV-medicijn dat niet hoeft te worden ingenomen met gepegyleerd interferon (peg-interferon) of ribavirine (twee geneesmiddelen die traditioneel worden gebruikt voor HCV-combinatietherapie, die beide een hoog toxiciteitsprofiel hadden).
Harvoni heeft naar verluidt genezingspercentages tussen 94% en 99%, terwijl fase II-onderzoeken een genezingspercentage van 100% hebben gemeld bij patiënten die gelijktijdig zijn geïnfecteerd met hiv en HCV.
Dosering
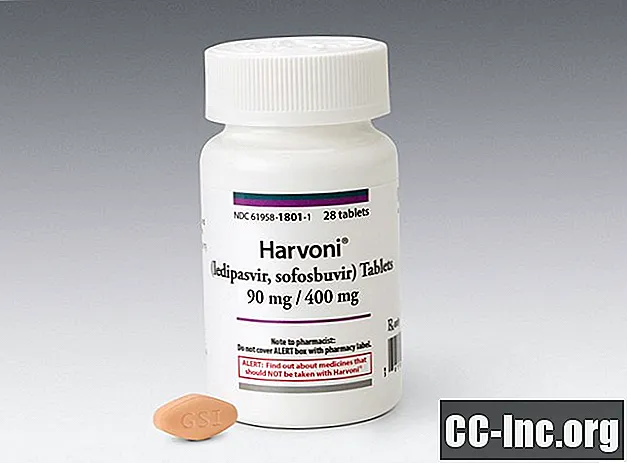
Eén tablet (90 mg / 400 mg) per dag ingenomen met of zonder voedsel. Harvoni-tabletten zijn ruitvormig, gemberkleurig en filmomhuld, met "GSI" in reliëf op de ene zijde en "7985" op de andere zijde.
Aanbevelingen voorschrijven
Harvoni wordt voorgeschreven voor een cursus van 12 tot 24 weken, volgens de volgende aanbevelingen:
- Nog niet eerder behandeld met of zonder cirrose: 12 weken
- Ervaren behandeling zonder cirrose: 12 weken
- Ervaren behandeling met cirrose: 24 weken
Bovendien kan een kuur van 8 weken worden overwogen voor behandelingsnaïeve patiënten zonder cirrose met een HCV-virale last van minder dan 6 miljoen kopieën / ml.
Vaak voorkomende bijwerkingen
De meest voorkomende bijwerkingen die verband houden met het gebruik van Harvoni (treden op bij 10% of minder van de patiënten) zijn:
- Vermoeidheid
- Hoofdpijn
Andere mogelijke bijwerkingen (minder dan 10%) zijn misselijkheid, diarree en slapeloosheid.
Geneesmiddelinteracties
Het volgende moet ook worden vermeden bij het gebruik van Harvoni:
- Op rifampicine gebaseerde medicijnen tegen tuberculose: Mycobutin, Rifater, Rifamate, Rimactane, Rifadin, Priftin
- Anticonvulsiva: Tegretol, Dilantin, Trileptal, fenobarbital
- Aptivus (tipranavir / ritonavir) gebruikt bij antiretrovirale hiv-therapie
- Sint-janskruid
Contra-indicaties en overwegingen
Er zijn geen contra-indicaties voor het gebruik van Harvoni bij patiënten met HCV-genotype 1.
Voor patiënten met hiv die het geneesmiddel tenofovir gebruiken (waaronder Viread, Truvada, Atripla, Complera, Stribild), moet echter extra aandacht worden besteed aan het controleren op eventuele bijwerkingen die met tenofovir verband houden, met name nier- (nier) stoornissen.
Antacida dienen 4 uur voor of na een Harvoni-dosis afzonderlijk te worden ingenomen, terwijl doseringen van protonpompremmers en H2-receptorremmers (ook bekend als H2-blokkers) mogelijk moeten worden verlaagd om een afnemende ledipasvirabsorptie te voorkomen.
Hoewel er geen contra-indicatie is voor het gebruik van Harvoni tijdens de zwangerschap, zijn er weinig klinische gegevens bij de mens beschikbaar. Dierstudies naar het gebruik van zowel ledipasvir als sofosbuvir hebben echter geen effect op de ontwikkeling van de foetus aangetoond. Tijdens de zwangerschap wordt consultatie door een specialist aanbevolen om de urgentie van de Harvoni-therapie te beoordelen, met name om onmiddellijk te beginnen of te wachten tot na de bevalling.
Het wordt aanbevolen om alle vrouwen in de vruchtbare leeftijd tijdens de behandeling maandelijks te controleren op zwangerschap. Het wordt ook aanbevolen om de patiënte en haar mannelijke partner ten minste twee niet-hormonale anticonceptiemethoden te geven en deze te gebruiken tijdens de therapie en gedurende zes maanden daarna.
Hepatitis C Doctor Discussiegids
Download onze afdrukbare gids voor uw volgende doktersafspraak om u te helpen de juiste vragen te stellen.

- Delen
- Omdraaien
- Tekst